Prawie 200 lat po odkryciu cząsteczki przez Michaela Faradaya naukowcy w końcu odkryli złożoną strukturę elektronową benzenu.
To nie tylko rozwiązuje trwającą od lat 30. kontrowersję, ale ma również ważne implikacje dla przyszłego rozwoju materiałów optoelektronicznych, z których wiele jest opartych na benzenie.
Struktura atomowa benzenu jest dość dobrze poznana. Jest to pierścień złożony z sześciu atomów węgla i sześciu atomów wodoru, po jednym na każdy atom węgla.
Staje się to niezwykle trudne, gdy weźmiemy pod uwagę 42 elektrony cząsteczki.
„Funkcja matematyczna opisująca elektrony benzenu jest 126-wymiarowa” – powiedział chemik Timothy Schmidt z ARC Centre of Excellence in Exciton Science i UNSW w Australii.
Oznacza to, że jest to funkcja 126 współrzędnych, po trzy dla każdego z 42 elektronów. Elektrony nie są niezależne, więc nie możemy tego rozbić na 42 niezależne funkcje 3D.
Odpowiedź maszyny nie jest łatwa do zinterpretowania przez ludzi i musieliśmy wymyślić sposób, aby uzyskać odpowiedź ”.
Oznacza to więc, że opis matematyczny struktury elektronowej benzenu musi uwzględniać 126 pomiarów. Jak możesz sobie wyobrazić, nie jest to łatwe. W rzeczywistości, ze względu na tę złożoność, odkrycie struktury pozostawało problemem przez tak długi czas, że doprowadziło do kontrowersji dotyczących zachowania elektronów benzenu.
Istnieją dwie szkoły myślenia: benzen opiera się na teorii wiązań walencyjnych ze zlokalizowanymi elektronami; lub teoria orbitali molekularnych z zdelokalizowanymi elektronami. Problem w tym, że żaden z nich nie wydaje się mieć racji.
„Interpretacja struktury elektronowej w kategoriach orbitali pomija fakt, że funkcja falowa jest antysymetryczna podczas wymiany tych samych spinów” – napisali naukowcy w artykule. „Co więcej, orbitale molekularne nie zapewniają intuicyjnego opisu korelacji elektronów”.
Praca zespołu opierała się na niedawno opracowanej technice. Nazywa się to dynamicznym próbkowaniem Voronoi Metropolis i wykorzystuje podejście algorytmiczne do wizualizacji funkcji falowych systemu wieloelektronowego.
Powoduje to podzielenie wymiarów elektronicznych na poszczególne kafelki diagramu Woronoja, gdzie każda z płytek odpowiada współrzędnym elektronicznym, umożliwiając zespołowi wyświetlenie funkcji falowej wszystkich 126 wymiarów.
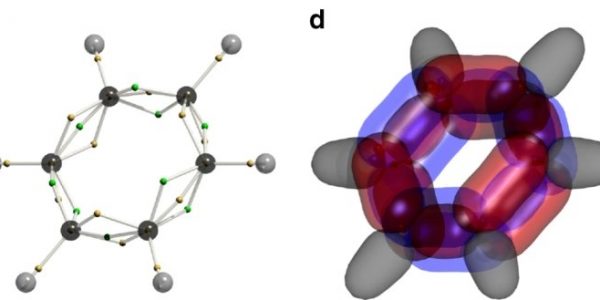
Przekrój cząsteczki. (Liu i in. Nature Communications, 2020)
I znaleźli coś dziwnego.
„Elektrony z tak zwanymi wiązaniami podwójnymi ze wzrostem prędkości obrotowej, gdzie elektrony z wiązaniami pojedynczymi ze spadkiem prędkości obrotowej i odwrotnie” – powiedział Schmidt. „Nie tak myślą chemicy o benzenie”.
W rezultacie elektrony unikają się nawzajem, gdy jest to korzystne, zmniejszając energię cząsteczki i czyniąc ją bardziej stabilną.
„Zasadniczo łączy ze sobą myślenie chemiczne, pokazując, jak łączą się dwa dominujące paradygmaty, których używamy do opisu benzenu” – powiedział.
„Ale pokazujemy również, jak przetestować tak zwaną korelację elektronów – jak elektrony unikają się nawzajem. Jest to prawie zawsze jakościowo pomijane i używane tylko do obliczeń, w których używana jest tylko energia, a nie zachowanie elektroniczne ”.
Badanie zostało opublikowane w Nature Communications.